เมื่อเร็วๆ นี้ สำนักงานคณะกรรมการอาหารและยาแห่งรัฐจีน (SFDA) ได้อนุมัติการยื่นขอจดทะเบียนยา tafolecimab (แอนติบอดีโมโนโคลนอล PCSK-9 ซึ่งผลิตโดย INNOVENT BIOLOGICS,INC), INC อย่างเป็นทางการสำหรับการรักษาภาวะไขมันในเลือดสูงชนิดปฐมภูมิ (รวมถึงภาวะไขมันในเลือดสูงแบบเฮเทอโรไซกัสทางพันธุกรรม และภาวะไขมันในเลือดสูงแบบไม่ใช่ทางพันธุกรรม) และภาวะไขมันในเลือดผิดปกติแบบผสม ยานี้เป็นยาต้าน PCSK-9 ที่ผลิตขึ้นเองตัวแรกที่ยื่นขอจดทะเบียนจำหน่ายในประเทศจีน
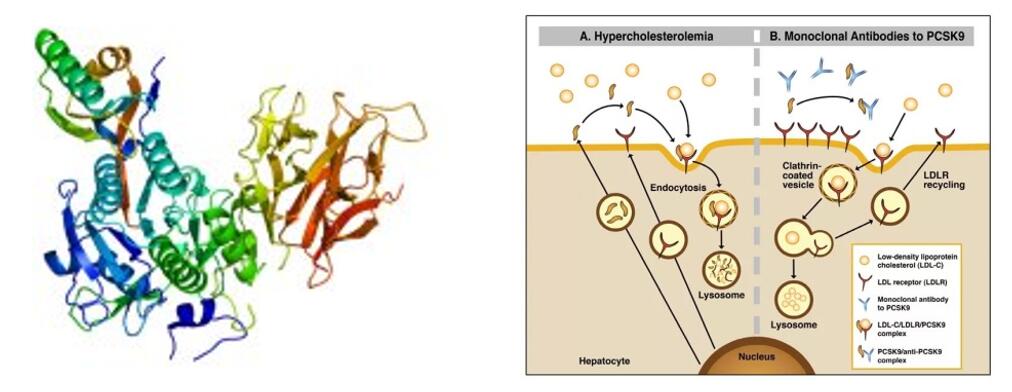
Tafolecimab เป็นยาชีวภาพเชิงนวัตกรรมที่พัฒนาขึ้นโดยอิสระโดย INNOVENT BIOLOGICS, INC. แอนติบอดีโมโนโคลนอล IgG2 ของมนุษย์จะจับกับ PCSK-9 โดยเฉพาะเพื่อเพิ่มระดับ LDLR โดยลดการรับเข้าเซลล์ที่เกิดจาก PCSK-9 ส่งผลให้การกำจัด LDL-C เพิ่มมากขึ้นและลดระดับ LDL-C ลง
ในช่วงไม่กี่ปีที่ผ่านมา อัตราการเกิดภาวะไขมันในเลือดผิดปกติได้เพิ่มขึ้นอย่างมีนัยสำคัญในประเทศจีน โดยอัตราการเกิดภาวะไขมันในเลือดผิดปกติและภาวะไขมันในเลือดสูงในผู้ใหญ่สูงถึง 40.4% และ 26.3% ตามลำดับ รายงานสุขภาพและโรคหลอดเลือดหัวใจในประเทศจีนปี 2563 ระบุว่า อัตราการรักษาและควบคุมภาวะไขมันในเลือดผิดปกติในผู้ใหญ่ยังคงอยู่ในระดับต่ำ และอัตราการปฏิบัติตามเกณฑ์ของ LDL-C ในผู้ป่วยภาวะไขมันในเลือดผิดปกติยิ่งต่ำลง
ก่อนหน้านี้ สแตตินเป็นยาหลักที่ใช้รักษาภาวะไขมันในเลือดสูงในประเทศจีน แต่ผู้ป่วยหลายรายยังคงไม่สามารถบรรลุเป้าหมายในการลดระดับ LDL-C หลังการรักษาได้ การนำ PCSK-9 ออกสู่ตลาดทำให้ผู้ป่วยได้รับประสิทธิภาพที่ดีขึ้น
การส่งยา tafolecimab จาก INNOVENT BIOLOGICS, INC อ้างอิงจากผลการทดลองทางคลินิก 3 ครั้งที่ลงทะเบียนในระยะทดลองแบบ democratic tafolecimab มีข้อมูลความปลอดภัยโดยรวมที่ดี คล้ายกับคุณลักษณะความปลอดภัยของผลิตภัณฑ์ที่วางจำหน่าย และมีระยะเวลาการให้ยาที่ยาวนาน (ทุก 6 สัปดาห์) ผลการศึกษา CREDIT-2 ได้รับการยอมรับให้เป็นบทคัดย่อในการประชุมประจำปี 2022 ของ American College of Cardiology (ACC) และเผยแพร่ทางออนไลน์
หากใบสมัครได้รับการอนุมัติ จะเป็นการทำลายทางตันของ PCSK-9 ที่ถูกบังคับใช้ โดยจีนจะกลายเป็นประเทศที่ 4 ที่มี PCSK-9 ต่อจากสหรัฐอเมริกา (Amgen) ฝรั่งเศส (Sanofi) และสวิตเซอร์แลนด์ (Novartis)
เวลาโพสต์: 4 ก.ค. 2565