Kiinan elintarvike- ja lääkevirasto (SFDA) hyväksyi hiljattain virallisesti tafolecimabin (INNOVENT BIOLOGICS,INC:n valmistaman PCSK-9-monoklonaalisen vasta-aineen) myyntiluvan primaarisen hyperkolesterolemian (mukaan lukien heterotsygoottinen familiaalinen hyperkolesterolemia ja ei-familiaalinen hyperkolesterolemia) ja sekamuotoisen dyslipidemian hoitoon. Tämä on ensimmäinen itse tuotettu PCSK-9-estäjä, jota on haettu markkinoille Kiinassa.
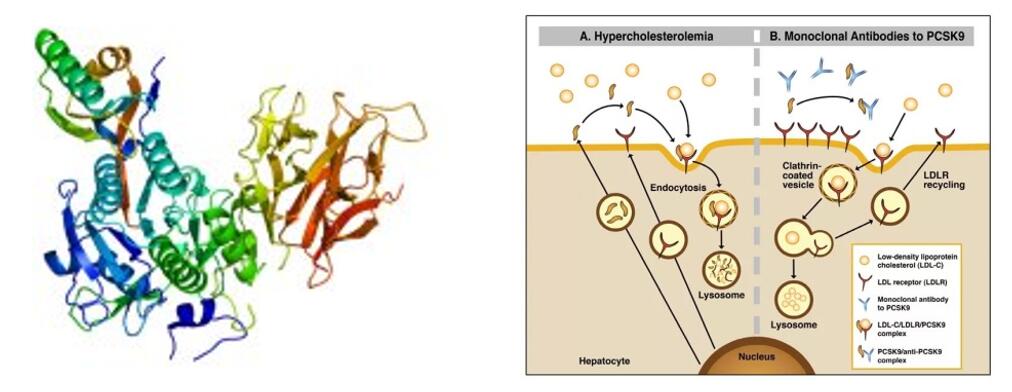
Tafolesimabi on innovatiivinen biologinen lääke, jonka INNOVENT BIOLOGICS, INC. on kehittänyt itsenäisesti. Ihmisen monoklonaalinen IgG2-vasta-aine sitoutuu spesifisesti PCSK-9:ään ja lisää LDLR-tasoja vähentämällä PCSK-9:n välittämää endosytoosia, mikä lisää LDL-kolesterolin poistumista ja alentaa LDL-kolesterolitasoja.
Viime vuosina dyslipidemian esiintyvyys on lisääntynyt merkittävästi Kiinassa. Dyslipidemian ja hyperkolesterolemian esiintyvyys aikuisilla on jopa 40,4 % ja 26,3 %. Vuoden 2020 Kiinan sydän- ja verisuoniterveyttä ja -sairauksia käsittelevän raportin mukaan dyslipidemian hoito- ja hallintaprosentti aikuisilla on edelleen alhainen, ja dyslipidemiapotilaiden LDL-kolesterolin hoitomyöntyvyyden taso on vieläkin epätyydyttävämpi.
Aiemmin statiinit olivat Kiinassa hyperkolesterolemian pääasiallinen hoitomuoto, mutta monet potilaat eivät vieläkään saavuttaneet LDL-kolesterolin alenemisen tavoitetta hoidon jälkeen. PCSK-9:n markkinoille tulo on tuonut potilaille paremman tehon.
INNOVENT BIOLOGICS, INC:n jättämä tafolecimabin hakemus perustuu kolmen demokraattisessa vaiheessa rekisteröidyn kliinisen tutkimuksen tuloksiin. Sillä on hyvä yleinen turvallisuusprofiili, joka on samanlainen kuin markkinoilla olevilla tuotteilla, ja sillä on saavutettu pitkät antovälit (6 viikon välein). American College of Cardiologyn (ACC) vuoden 2022 vuosikokous hyväksyi CREDIT-2-tutkimuksen tulokset abstraktina ja julkaisi ne verkossa.
Jos hakemus hyväksytään, se rikkoo PCSK-9:n käyttöönoton umpikujan ja Kiinasta tulee neljäs maa, jossa on PCSK-9:ää, Yhdysvaltojen (Amgen), Ranskan (Sanofi) ja Sveitsin (Novartis) jälkeen.
Julkaisun aika: 04.07.2022