Onlangs heeft de Chinese State Food and Drug Administration (SFDA) officieel de aanvraag voor het op de markt brengen van tafolecimab (een monoklonaal antilichaam PCSK-9, geproduceerd door INNOVENT BIOLOGICS, INC.) goedgekeurd voor de behandeling van primaire hypercholesterolemie (inclusief heterozygote familiaire hypercholesterolemie en niet-familiaire hypercholesterolemie) en gemengde dyslipidemie. Dit is de eerste zelfgeproduceerde PCSK-9-remmer die een aanvraag voor marktintroductie in China heeft ingediend.
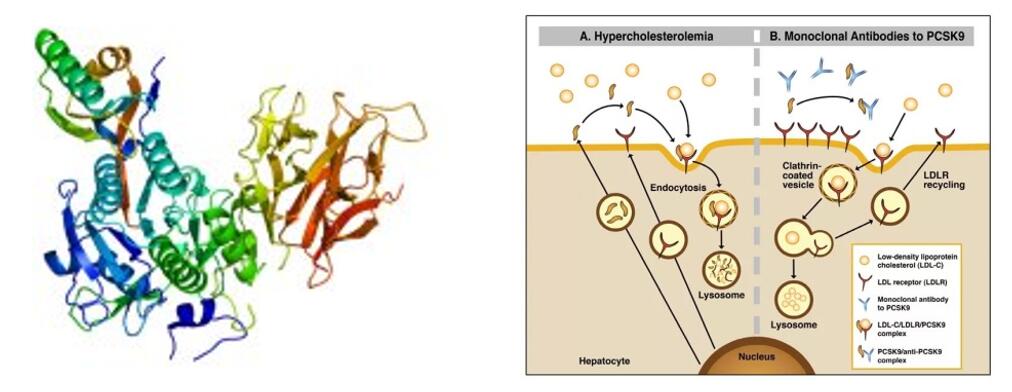
Tafolecimab is een innovatief biologisch geneesmiddel dat onafhankelijk is ontwikkeld door INNOVENT BIOLOGICS, INC. Het IgG2-monoklonale antilichaam voor mensen bindt zich specifiek aan PCSK-9 om de LDLR-niveaus te verhogen door de door PCSK-9 gemedieerde endocytose te verminderen, waardoor de eliminatie van LDL-C wordt verhoogd en de LDL-C-niveaus worden verlaagd.
De prevalentie van dyslipidemie is de afgelopen jaren in China aanzienlijk toegenomen. De prevalentie van dyslipidemie en hypercholesterolemie bij volwassenen bedraagt respectievelijk 40,4% en 26,3%. Volgens het rapport over cardiovasculaire gezondheid en ziekten in China uit 2020 liggen de behandelings- en controlepercentages van dyslipidemie bij volwassenen nog steeds op een laag niveau, en is de naleving van de LDL-C-richtlijnen bij patiënten met dyslipidemie nog minder bevredigend.
Voorheen waren statines de belangrijkste behandeling voor hypercholesterolemie in China, maar veel patiënten slaagden er nog steeds niet in om het beoogde doel van LDL-C-verlaging na behandeling te bereiken. De marketing van PCSK-9 heeft geleid tot een betere werkzaamheid voor patiënten.
De indiening van tafolecimab door INNOVENT BIOLOGICS, INC. is gebaseerd op de resultaten van drie klinische onderzoeken die in een democratisch stadium zijn geregistreerd. Het heeft een goed algemeen veiligheidsprofiel, vergelijkbaar met de veiligheidskenmerken van op de markt gebrachte producten, en heeft lange toedieningsintervallen (elke 6 weken) bereikt. De resultaten van de CREDIT-2-studie werden door de jaarlijkse bijeenkomst van het American College of Cardiology (ACC) in 2022 als samenvatting geaccepteerd en online gepubliceerd.
Als de aanvraag wordt goedgekeurd, wordt de impasse rondom het verboden PCSK-9 doorbroken. China wordt dan het vierde land met PCSK-9, na de Verenigde Staten (Amgen), Frankrijk (Sanofi) en Zwitserland (Novartis).
Plaatsingstijd: 4 juli 2022