Di recente, la Food and Drug Administration (SFDA) cinese ha ufficialmente accettato la domanda di autorizzazione all'immissione in commercio di tafolecimab (anticorpo monoclonale PCSK-9 prodotto da INNOVENT BIOLOGICS, INC), per il trattamento dell'ipercolesterolemia primaria (inclusa l'ipercolesterolemia familiare eterozigote e l'ipercolesterolemia non familiare) e della dislipidemia mista. Si tratta del primo inibitore PCSK-9 autoprodotto a presentare domanda di autorizzazione all'immissione in commercio in Cina.
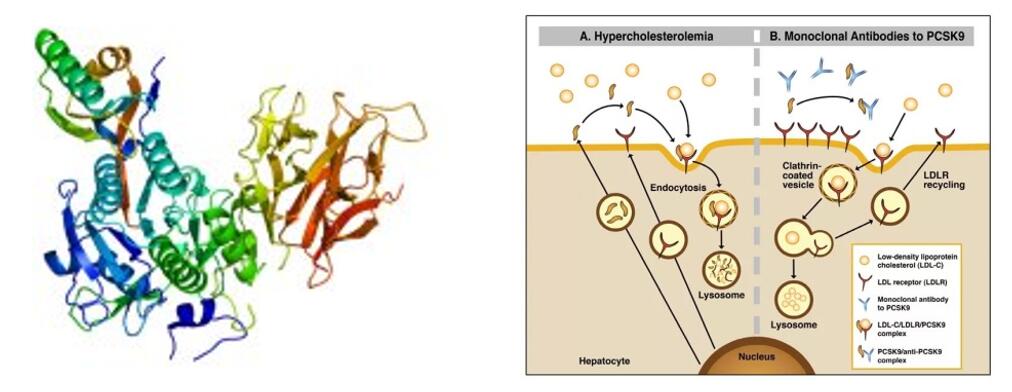
Il tafolecimab è un farmaco biologico innovativo sviluppato in modo indipendente da INNOVENT BIOLOGICS, INC. L'anticorpo monoclonale umano IgG2 si lega specificamente al PCSK-9 per aumentare i livelli di LDLR riducendo l'endocitosi mediata dal PCSK-9, aumentando così l'eliminazione dell'LDL-C e abbassando i livelli di LDL-C.
Negli ultimi anni, la prevalenza della dislipidemia è aumentata significativamente in Cina. La prevalenza di dislipidemia e ipercolesterolemia negli adulti raggiunge rispettivamente il 40,4% e il 26,3%. Secondo il rapporto del 2020 sulla salute e le malattie cardiovascolari in Cina, il tasso di trattamento e controllo della dislipidemia negli adulti è ancora basso e il tasso di compliance dei pazienti con dislipidemia è ancora meno soddisfacente.
In precedenza, le statine erano il trattamento principale per l'ipercolesterolemia in Cina, ma molti pazienti non riuscivano ancora a raggiungere l'obiettivo terapeutico di riduzione del colesterolo LDL dopo il trattamento. La commercializzazione di PCSK-9 ha migliorato l'efficacia per i pazienti.
La presentazione del tafolecimab da parte di INNOVENT BIOLOGICS, INC. si basa sui risultati di tre studi clinici registrati in fase democratica. Presenta un buon profilo di sicurezza complessivo, simile alle caratteristiche di sicurezza dei prodotti commercializzati, e ha raggiunto intervalli di somministrazione prolungati (ogni 6 settimane). I risultati dello studio CREDIT-2 sono stati accettati come abstract dal Congresso Annuale 2022 dell'American College of Cardiology (ACC) e pubblicati online.
Se la domanda verrà approvata, si romperà la situazione di stallo del PCSK-9 imposto, e la Cina diventerà il quarto paese ad avere il PCSK-9 dopo gli Stati Uniti (Amgen), la Francia (Sanofi) e la Svizzera (Novartis).
Data di pubblicazione: 04-07-2022