Hiljuti kiitis Hiina Riiklik Toidu- ja Ravimiamet (SFDA) ametlikult heaks tafoletsimabi (PCSK-9 monoklonaalne antikeha, mida toodab INNOVENT BIOLOGICS, INC), INC turustamistaotluse primaarse hüperkolesteroleemia (sealhulgas heterosügootse perekondliku hüperkolesteroleemia ja mitteperekondliku hüperkolesteroleemia) ja segatüüpi düslipideemia raviks. See on esimene isetoodetud PCSK-9 inhibiitor, mille turustamist Hiinas taotletakse.
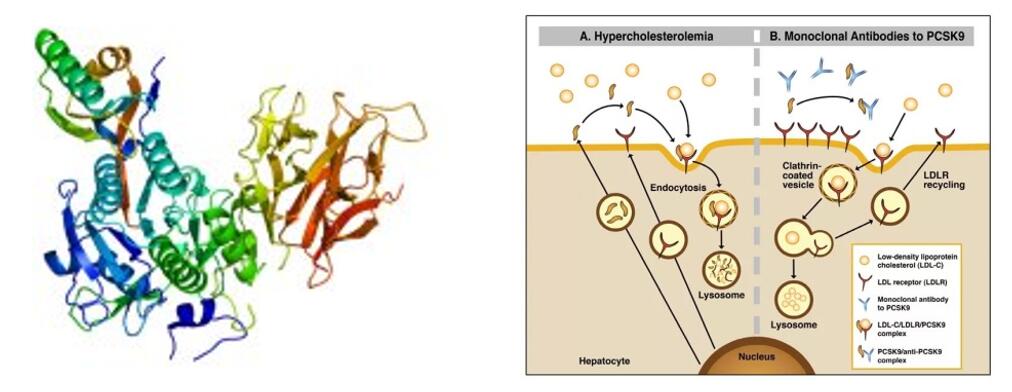
Tafoletsimab on uuenduslik bioloogiline ravim, mille on iseseisvalt välja töötanud INNOVENT BIOLOGICS, INC. Inimese monoklonaalne IgG2 antikeha seondub spetsiifiliselt PCSK-9-ga, et suurendada LDLR taset, vähendades PCSK-9 vahendatud endotsütoosi, suurendades seeläbi LDL-kolesterooli eliminatsiooni ja alandades LDL-kolesterooli taset.
Viimastel aastatel on düslipideemia levimus Hiinas märkimisväärselt suurenenud. Düslipideemia ja hüperkolesteroleemia levimus täiskasvanutel on vastavalt 40,4% ja 26,3%. 2020. aasta aruande kohaselt südame-veresoonkonna tervise ja haiguste kohta Hiinas on düslipideemia ravi ja kontrolli määr täiskasvanutel endiselt madal ning düslipideemiaga patsientide LDL-kolesterooli ravi järgimise määr on veelgi vähem rahuldav.
Varem olid Hiinas hüperkolesteroleemia peamiseks raviks statiinid, kuid paljud patsiendid ei suutnud ravi järel ikkagi saavutada LDL-kolesterooli vähendamise eesmärki. PCSK-9 turustamine on patsientidele paremat efektiivsust toonud.
INNOVENT BIOLOGICS, INC esitatud tafoletsimabi taotlus põhineb kolme demokraatlikus etapis registreeritud kliinilise uuringu tulemustel. Sellel on hea üldine ohutusprofiil, mis sarnaneb turustatavate toodete ohutusomadustega, ning see on saavutanud pikad manustamisintervallid (iga 6 nädala järel). CREDIT-2 uuringu tulemused kiideti heaks Ameerika Kardioloogiakolledži (ACC) 2022. aasta aastakoosolekul kokkuvõttena ja avaldati veebis.
Kui taotlus heaks kiidetakse, murrab see PCSK-9 impeerimise ummikseisu ning Hiinast saab neljas riik, kus PCSK-9 on, pärast Ameerika Ühendriike (Amgen), Prantsusmaad (Sanofi) ja Šveitsi (Novartis).
Postituse aeg: 04.07.2022