Recentemente, l'Amministrazione Statale Cinese per l'Alimentazione è i Medicinali (SFDA) hà accettatu ufficialmente a dumanda di cummercializazione di tafolecimab (anticorpu monoclonale PCSK-9 fabbricatu da INNOVENT BIOLOGICS,INC), INC per u trattamentu di l'ipercolesterolemia primaria (cumprese l'ipercolesterolemia familiare eterozigote è l'ipercolesterolemia non familiare) è a dislipidemia mista. Questu hè u primu inhibitore PCSK-9 autoproduttu à dumandà a cummercializazione in Cina.
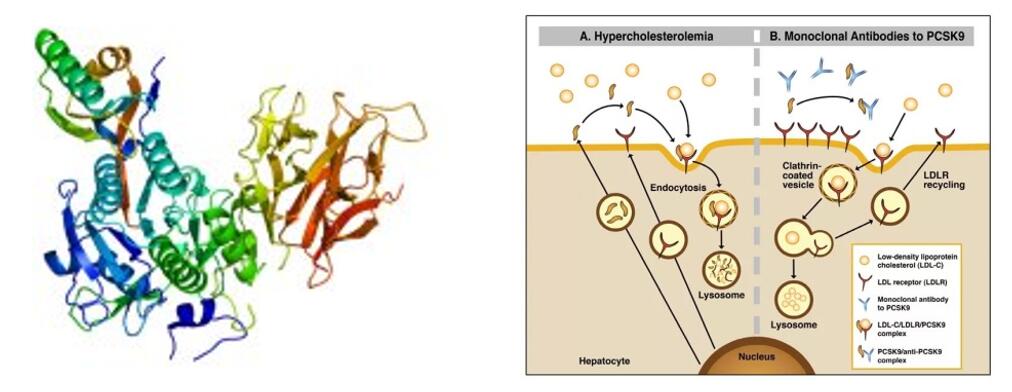
Tafolecimab hè una droga biologica innovativa sviluppata indipindentamente da INNOVENT BIOLOGICS, INC. L'anticorpu monoclonale umanu IgG2 si lega specificamente à PCSK-9 per aumentà i livelli di LDLR riducendu l'endocitosi mediata da PCSK-9, aumentendu cusì l'eliminazione di LDL-C è riducendu i livelli di LDL-C.
In l'ultimi anni, a prevalenza di a dislipidemia hè aumentata significativamente in Cina. A prevalenza di a dislipidemia è di l'ipercolesterolemia in l'adulti hè rispettivamente di 40,4% è 26,3%. Sicondu u rapportu di u 2020 nantu à a Salute è e Malatie Cardiovasculari in Cina, u tassu di trattamentu è di cuntrollu di a dislipidemia in l'adulti hè sempre à un livellu bassu, è u tassu di cunfurmità cù u LDL-C di i pazienti cun dislipidemia hè ancu menu soddisfacente.
Prima, e statine eranu u trattamentu principale per l'ipercolesterolemia in Cina, ma parechji pazienti ùn anu ancu riesciutu à ottene l'ubbiettivu di trattamentu di riduzione di LDL-C dopu u trattamentu. A cummercializazione di PCSK-9 hà purtatu una migliore efficacia à i pazienti.
A presentazione di tafolecimab da INNOVENT BIOLOGICS, INC hè basata annantu à i risultati di trè studii clinichi registrati in una fase demucratica. Hà un bonu prufilu di sicurezza generale, simile à e caratteristiche di sicurezza di i prudutti cummercializati, è hà ottenutu intervalli longhi (ogni 6 settimane) di amministrazione. I risultati di u studiu CREDIT-2 sò stati accettati da a Riunione Annuale 2022 di l'American College of Cardiology (ACC) cum'è un riassuntu è publicati in linea.
Sè a dumanda hè appruvata, romperà u stallo di PCSK-9 impostu, a Cina diventerà u quartu paese à avè PCSK-9 dopu à i Stati Uniti (Amgen), a Francia (Sanofi) è a Svizzera (Novartis).
Data di publicazione: 04-lugliu-2022