Recentment, l'Administració Estatal d'Aliments i Medicaments de la Xina (SFDA) ha acceptat oficialment la sol·licitud de comercialització de tafolecimab (anticòs monoclonal PCSK-9 fabricat per INNOVENT BIOLOGICS,INC), INC per al tractament de la hipercolesterolèmia primària (inclosa la hipercolesterolèmia familiar heterozigòtica i la hipercolesterolèmia no familiar) i la dislipèmia mixta. Aquest és el primer inhibidor de PCSK-9 de producció pròpia que sol·licita la seva comercialització a la Xina.
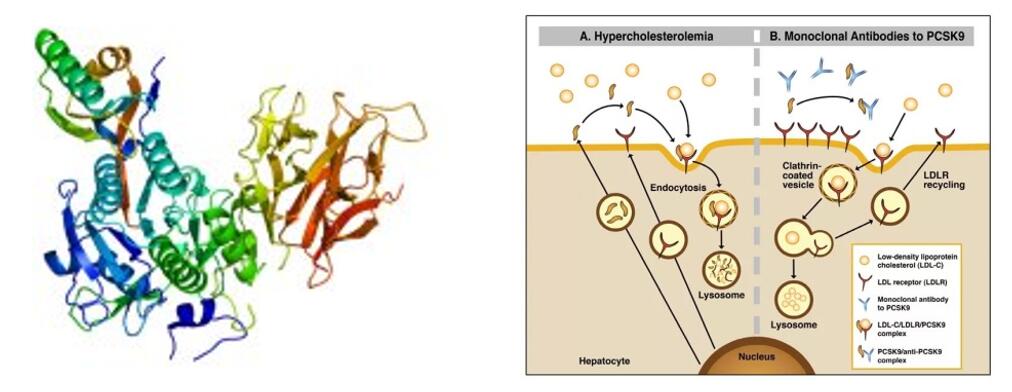
El tafolecimab és un fàrmac biològic innovador desenvolupat independentment per INNOVENT BIOLOGICS, INC. L'anticòs monoclonal humà IgG2 s'uneix específicament a PCSK-9 per augmentar els nivells de LDLR mitjançant la reducció de l'endocitosi mediada per PCSK-9, augmentant així l'eliminació de LDL-C i reduint els nivells de LDL-C.
En els darrers anys, la prevalença de la dislipèmia ha augmentat significativament a la Xina. La prevalença de la dislipèmia i la hipercolesterolèmia en adults arriba al 40,4% i al 26,3%, respectivament. Segons l'informe del 2020 sobre salut i malalties cardiovasculars a la Xina, la taxa de tractament i control de la dislipèmia en adults encara es troba a un nivell baix, i la taxa de compliment del colesterol LDL dels pacients amb dislipèmia és encara menys satisfactòria.
Anteriorment, les estatines eren el principal tractament per a la hipercolesterolèmia a la Xina, però molts pacients encara no aconseguien l'objectiu de reducció del LDL-C després del tractament. La comercialització de PCSK-9 ha aportat una millor eficàcia als pacients.
La presentació de tafolecimab per part d'INNOVENT BIOLOGICS, INC es basa en els resultats de tres assajos clínics registrats en fase democràtica. Té un bon perfil de seguretat general, similar a les característiques de seguretat dels productes comercialitzats, i ha aconseguit intervals llargs (cada 6 setmanes) d'administració. Els resultats de l'estudi CREDIT-2 van ser acceptats per la Reunió Anual de 2022 de l'American College of Cardiology (ACC) com a resum i publicats en línia.
Si la sol·licitud és aprovada, es trencarà el bloqueig de la PCSK-9 imposada, i la Xina es convertirà en el quart país a tenir PCSK-9 després dels Estats Units (Amgen), França (Sanofi) i Suïssa (Novartis).
Data de publicació: 04-07-2022