Onlangs het die Chinese Staatsvoedsel- en Medisyne-administrasie (SFDA) amptelik die bemarkingsaansoek van tafolecimab (PCSK-9 Monoklonale teenliggaam wat deur INNOVENT BIOLOGICS,INC), INC vervaardig word, vir die behandeling van primêre hipercholesterolemie (insluitend heterosigotiese familiële hipercholesterolemie en nie-familiale hipercholesterolemie) en gemengde dislipidemie aanvaar. Dit is die eerste selfvervaardigde PCSK-9-inhibeerder wat vir bemarking in China aansoek gedoen het.
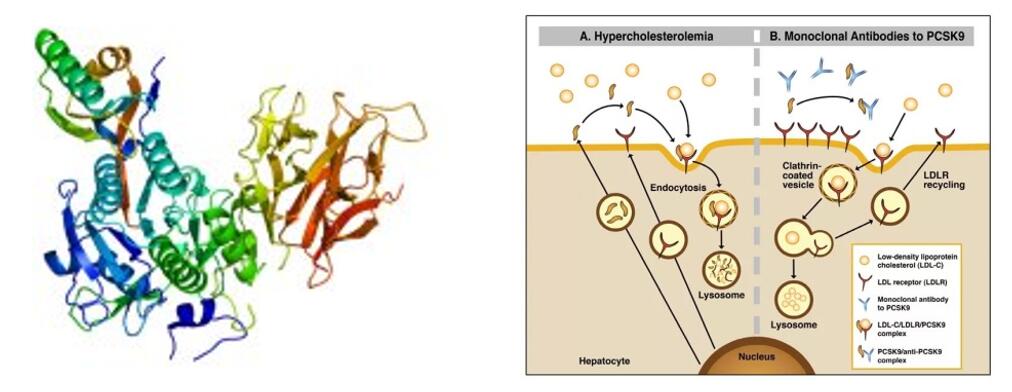
Tafolecimab is 'n innoverende biologiese middel wat onafhanklik ontwikkel is deur INNOVENT BIOLOGICS, INC. IgG2 menslike monoklonale teenliggaam bind spesifiek PCSK-9 om LDLR-vlakke te verhoog deur PCSK-9-gemedieerde endositose te verminder, waardeur LDL-C-eliminasie verhoog word en LDL-C-vlakke verlaag word.
In onlangse jare het die voorkoms van dislipidemie aansienlik in China toegeneem. Die voorkoms van dislipidemie en hipercholesterolemie by volwassenes is so hoog as onderskeidelik 40,4% en 26,3%. Volgens die 2020-verslag oor kardiovaskulêre gesondheid en siektes in China is die behandelings- en beheerkoers van dislipidemie by volwassenes steeds op 'n lae vlak, en die LDL-C-nakomingskoers van dislipidemie-pasiënte is selfs minder bevredigend.
Voorheen was statiene die hoofbehandeling vir hipercholesterolemie in China, maar baie pasiënte het steeds nie die behandelingsteiken van LDL-C-verlaging na behandeling bereik nie. Die bemarking van PCSK-9 het beter doeltreffendheid vir pasiënte gebring.
Die voorlegging van tafolecimab deur INNOVENT BIOLOGICS, INC is gebaseer op die resultate van drie kliniese proewe wat in 'n demokratiese stadium geregistreer is. Dit het 'n goeie algehele veiligheidsprofiel, soortgelyk aan die veiligheidseienskappe van bemarkte produkte, en het lang tussenposes (elke 6 weke) van toediening bereik. Die resultate van die CREDIT-2-studie is deur die 2022 Jaarlikse Vergadering van die Amerikaanse Kollege vir Kardiologie (ACC) as 'n abstrak aanvaar en aanlyn gepubliseer.
Indien die aansoek goedgekeur word, sal dit die dooiepunt van die geïmplementeerde PCSK-9 verbreek, en China sal die vierde land word wat PCSK-9 het na die Verenigde State (Amgen), Frankryk (Sanofi) en Switserland (Novartis).
Plasingstyd: 4 Julie 2022