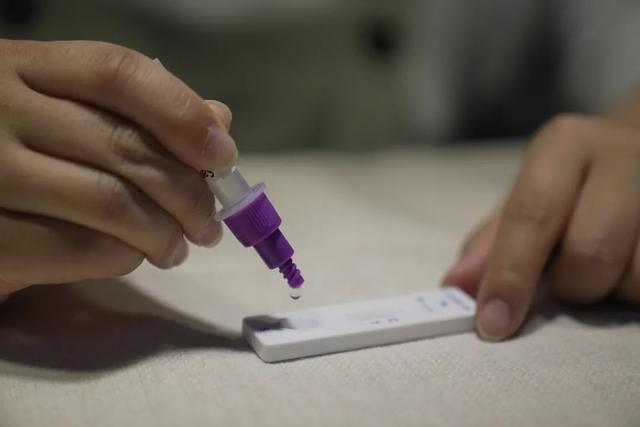
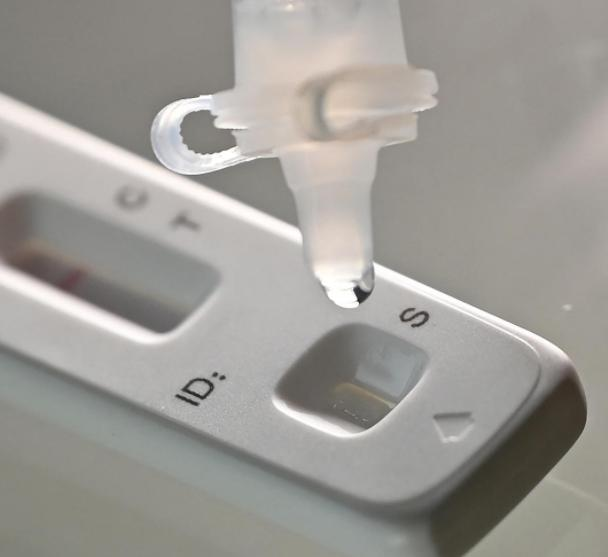
วันที่ 12 มีนาคมth ปี 2022, การเอ็นเอ็มพีเอ (SFDA) ออกประกาศอนุมัติการเปลี่ยนแปลงการขอตรวจผลิตภัณฑ์แอนติเจนโควิด-19 ด้วยตนเองโดย Nanjing Vazyme Biotechบริษัท จำกัดเทคโนโลยีวิศวกรรมชีวภาพปักกิ่งจินหวู่ฟู่บริษัท จำกัด, บริษัท เซินเจิ้น หัวต้า หยินหยวน ฟาร์มาซูติคอล เทคโนโลยี จำกัด, บริษัท กวางโจว วอนโฟ ไบโอเทค จำกัด และBบริษัท อี้จิง ซาวองต์ ไบโอเทคโนโลยี จำกัด(หัวkeไท)ได้เปิดตัวผลิตภัณฑ์ทดสอบแอนติเจน COVID-19 ด้วยตนเองจำนวน 5 รายการ
เมื่อวันที่ 11 มีนาคม 2565 คณะกรรมการสุขภาพแห่งชาติ (NHC) ได้ประกาศว่า เพื่อเพิ่มประสิทธิภาพกลยุทธ์การตรวจหาเชื้อไวรัสโคโรนาสายพันธุ์ใหม่ให้เหมาะสมยิ่งขึ้น และตอบสนองความต้องการในการป้องกันและควบคุมโควิด-19 คณะทำงานครอบคลุมของกลไกการป้องกันและควบคุมร่วมของคณะรัฐมนตรีได้ตัดสินใจเพิ่มการทดสอบแอนติเจนในการทดสอบกรดนิวคลีอิก และจัดทำ “พิธีสารการประยุกต์สำหรับการตรวจหาแอนติเจนของไวรัสโคโรนาสายพันธุ์ใหม่ (การทดลอง)”
โปรโตคอลระบุประชากรที่ใช้สำหรับการทดสอบแอนติเจน:
1. ผู้ที่ไปรับบริการที่สถานพยาบาลเบื้องต้นแล้วมีอาการ เช่น ทางเดินหายใจ มีไข้ ภายใน 5 วัน นับจากวันเริ่มมีอาการ
ประการที่สอง เจ้าหน้าที่สังเกตการณ์กักกันตัว ได้แก่ เจ้าหน้าที่สังเกตการณ์กักกันตัวที่บ้าน เจ้าหน้าที่สังเกตการณ์สัมผัสใกล้ชิดและสัมผัสกึ่งใกล้ชิด เจ้าหน้าที่สังเกตการณ์กักกันตัวขณะเข้าประเทศ เจ้าหน้าที่พื้นที่กักกันตัวและเจ้าหน้าที่พื้นที่ควบคุม
ประการที่สาม คือ ประชาชนในชุมชนที่มีความต้องการตรวจหาแอนติเจนด้วยตนเอง
เคล็ดลับ: การตรวจหาแอนติเจนเป็นส่วนเสริมที่สำคัญของการตรวจหากรดนิวคลีอิก แต่ผลการตรวจแอนติเจนด้วยตนเองไม่สามารถใช้เป็นพื้นฐานในการวินิจฉัยการติดเชื้อได้
เวลาโพสต์: 22 มี.ค. 2565