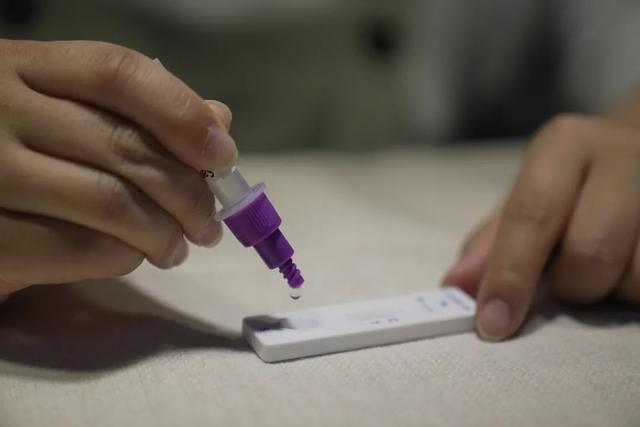
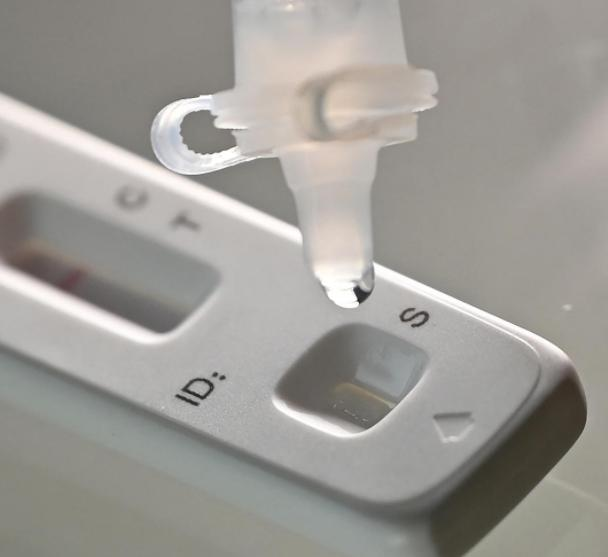
12. marcath 2022, taNMPA (SFDA) izdal obvestilo o odobritvi spremembe vloge za samotestiranje izdelkov z antigenom COVID-19 s strani podjetja Nanjing Vazyme Biotechd.o.o., Pekinška tehnologija bioinženiringa Jinwofud.o.o., Shenzhen Huada Yinyuan Farmacevtska tehnologija Co., Ltd., Guangzhou Wondfo Biotech Co., Ltd. inBeijing Savant Biotechnology Co., Ltd.(Huaketaj)Na trg je bilo lansiranih pet izdelkov za samotestiranje antigena COVID-19.
NHC je 11. marca 2022 sporočil, da se je celovita ekipa skupnega mehanizma za preprečevanje in nadzor državnega sveta odločila, da bo testiranju nukleinskih kislin dodala še antigensko testiranje in pripravila „Protokol za odkrivanje antigena novega koronavirusa (preskušanje)“, da bi dodatno optimizirala strategijo testiranja za novi koronavirus in zadostila potrebam preprečevanja in obvladovanja COVID-19.
Protokol določa ustrezno populacijo za testiranje antigena:
Prvič, tisti, ki obiščejo primarne zdravstvene ustanove in imajo simptome, kot so težave z dihali in vročina, v 5 dneh od pojava simptomov;
Drugič, osebje za opazovanje v karanteni, vključno z opazovanjem v domači karanteni, osebjem v tesnem in podtesnem stiku, osebjem v vstopni karanteni, osebjem v zadrževalnem območju in nadzornem območju;
Tretji so prebivalci skupnosti, ki potrebujejo samozaznavanje antigenov.
Nasveti: Detekcija antigena je pomemben dodatek k detekciji nukleinskih kislin, vendar rezultatov samodetekcije antigena ni mogoče uporabiti kot osnovo za diagnozo okužbe.
Čas objave: 22. marec 2022