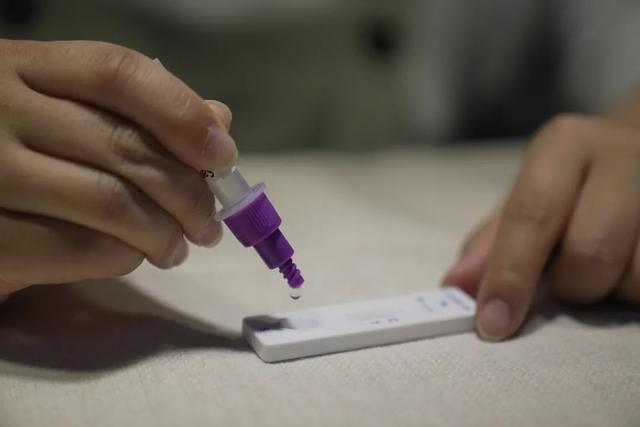
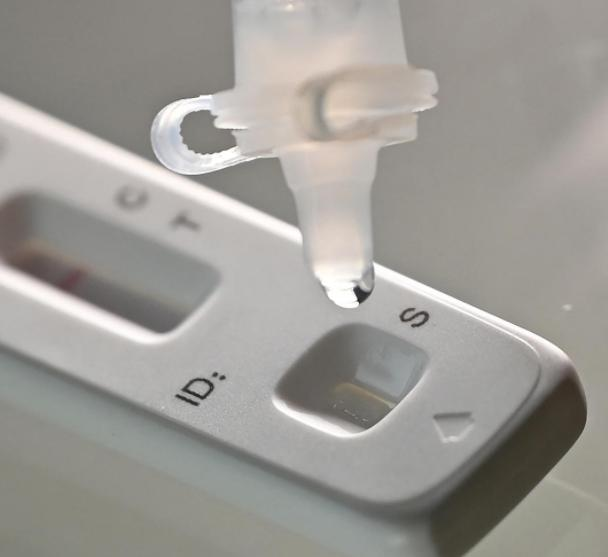
Pe 12 martieth 2022, cel/cea/cei/celeNMPA (SFDA) a emis o notificare prin care aprobă modificarea aplicației pentru autotestarea produselor antigenice COVID-19 de către Nanjing Vazyme BiotechCo., Ltd., Tehnologia de Bioinginerie Jinwofu din BeijingCo., Ltd., Shenzhen Huada Yinyuan Tehnologie Farmaceutică Co., Ltd., Guangzhou Wondfo Biotech Co., Ltd. şiBEijing Savant Biotechnology Co., Ltd.(Huaketai)Au fost lansate cinci produse de autotestare a antigenului COVID-19.
Pe 11 martie 2022, NHC a anunțat că, pentru a optimiza în continuare strategia de testare a noului coronavirus și pentru a satisface nevoile de prevenire și control al COVID-19, Echipa cuprinzătoare a mecanismului comun de prevenire și control al Consiliului de Stat a decis să adauge testarea antigenului la testarea acidului nucleic și a elaborat „Protocolul de aplicare pentru detectarea antigenului noului coronavirus (studiu)”.
Protocolul specifică populația aplicabilă pentru testarea antigenului:
În primul rând, cei care se prezintă la instituții medicale primare și prezintă simptome precum simptome respiratorii și febră în decurs de 5 zile de la debutul simptomelor;
În al doilea rând, personalul de observare a carantinei, inclusiv personalul de observare a carantinei la domiciliu, personalul de contact apropiat și sub-apropiat, personalul de observare a carantinei la intrare, personalul din zona de izolare și personalul din zona de control;
Al treilea sunt locuitorii comunității care au nevoie de autodetectare a antigenului.
Sfaturi: Detectarea antigenului este un supliment important al detectării acidului nucleic, dar rezultatele autodetectării antigenului nu pot fi utilizate ca bază pentru diagnosticarea infecției.
Data publicării: 22 martie 2022