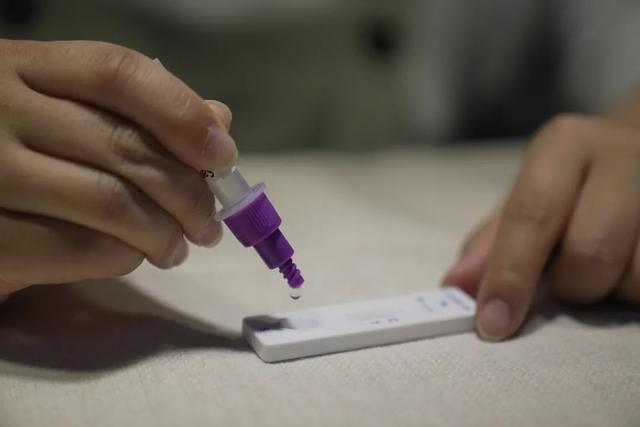
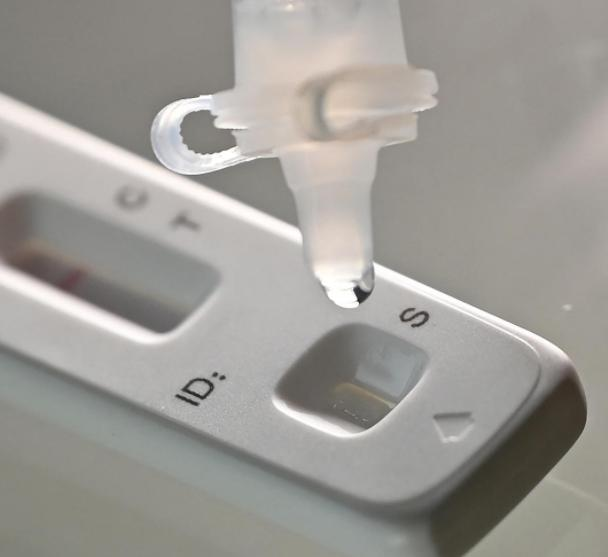
در ۱۲ مارسth ۲۰۲۲، ...NMPA (SFDA) اطلاعیهای مبنی بر تأیید تغییر درخواست برای خودآزمایی محصولات آنتیژن کووید-۱۹ توسط شرکت نانجینگ وازیم بیوتکنولوژی صادر کرد.شرکت با مسئولیت محدود، فناوری مهندسی زیستی پکن جینووفوشرکت با مسئولیت محدود, شرکت فناوری دارویی شنژن هوآدا یینیوان، با مسئولیت محدود, شرکت بیوتکنولوژی گوانگژو ووندفو وBشرکت بیوتکنولوژی ساوانت ایجینگ، با مسئولیت محدود(هوآkeتای)پنج محصول خودآزمایی آنتیژن کووید-۱۹ به بازار عرضه شدهاند.
در ۱۱ مارس ۲۰۲۲، کمیسیون ملی بهداشت (NHC) اعلام کرد که به منظور بهینهسازی بیشتر استراتژی آزمایش ویروس کرونای جدید و تأمین نیازهای پیشگیری و کنترل کووید-۱۹، تیم جامع مکانیسم مشترک پیشگیری و کنترل شورای دولتی تصمیم گرفت آزمایش آنتیژن را به آزمایش اسید نوکلئیک اضافه کند و «پروتکل کاربردی برای تشخیص آنتیژن ویروس کرونای جدید (آزمایشی)» را تدوین کرد.
این پروتکل جمعیت مورد نظر برای آزمایش آنتیژن را مشخص میکند:
اول، کسانی که به مراکز درمانی اولیه مراجعه میکنند و علائمی مانند مشکلات تنفسی و تب را ظرف ۵ روز از شروع علائم دارند؛
دوم، پرسنل نظارت بر قرنطینه، شامل نظارت بر قرنطینه خانگی، افراد در تماس نزدیک و افراد در تماس نزدیک، نظارت بر قرنطینه ورودی، پرسنل منطقه مهار و منطقه کنترل؛
گروه سوم، ساکنان جامعه هستند که نیاز به خودآزمایی آنتیژن دارند.
نکات: تشخیص آنتیژن مکمل مهمی برای تشخیص اسید نوکلئیک است، اما نتایج تشخیص خودبهخودی آنتیژن نمیتواند به عنوان مبنایی برای تشخیص عفونت استفاده شود.
زمان ارسال: ۲۲ مارس ۲۰۲۲