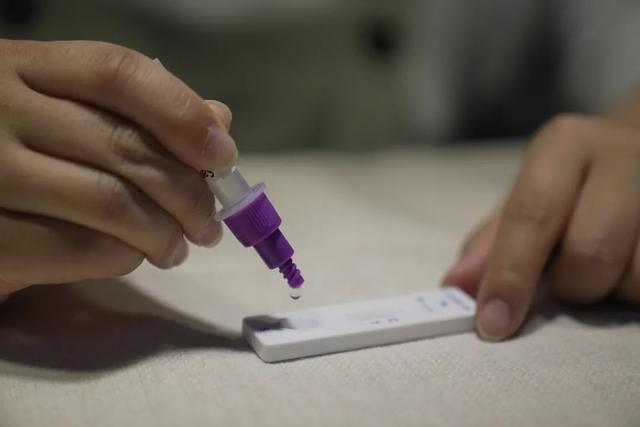
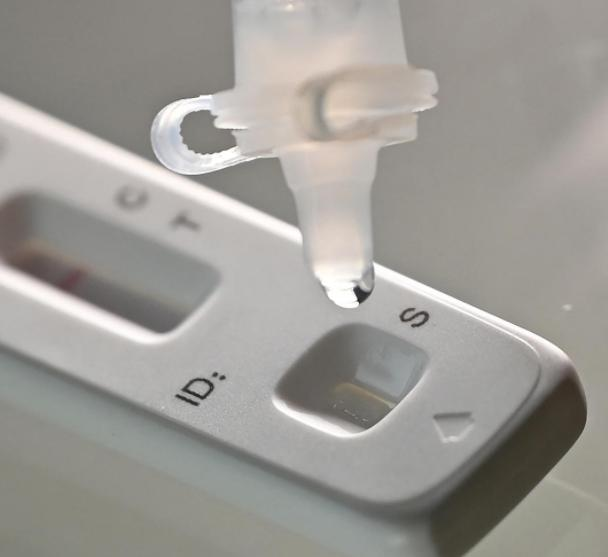
Den 12. martsth 2022, deNMPA (SFDA) udstedte en meddelelse om godkendelse af ændringen af ansøgningen om selvtestning af COVID-19-antigenprodukter fra Nanjing Vazyme BiotechCo., Ltd.Beijing Jinwofu Bioengineering TechnologyCo., Ltd., Shenzhen Huada Yinyuan Pharmaceutical Technology Co., Ltd., Guangzhou Wondfo Biotech Co., Ltd. ogBEijing Savant Biotechnology Co., Ltd.(Huaketai)Fem produkter til selvtestning af COVID-19-antigen er blevet lanceret.
Den 11. marts 2022 meddelte NHC, at det omfattende team under Statsrådets fælles forebyggelses- og kontrolmekanisme (JFM) for yderligere at optimere teststrategien for den nye coronavirus og imødekomme behovene for COVID-19-forebyggelse og -kontrol, besluttede at tilføje antigentestning til nukleinsyretestning og udarbejdede en "anvendelsesprotokol til påvisning af antigen fra nye coronavirus (forsøg)".
Protokollen specificerer den relevante population til antigentestning:
For det første dem, der besøger primære lægeinstitutioner og har symptomer som luftvejsinfektioner og feber inden for 5 dage efter symptomernes debut;
For det andet, karantæneobservationspersonale, herunder observation i hjemmekarantæne, tæt kontakt og subtæt kontakt, observation i indrejsekarantæne, personale i inddæmningsområder og kontrolområder;
Den tredje er beboerne i lokalsamfundet, som har behov for selvdetektion af antigen.
Tips: Antigendetektion er et vigtigt supplement til nukleinsyredetektion, men resultaterne af antigen-selvdetektion kan ikke bruges som grundlag for diagnosen af infektion.
Opslagstidspunkt: 22. marts 2022